摘 要 邻苯二甲酸酯为人类提供高品质塑料制品中的作用不可或缺,但其同时也可致癌。本文对邻苯二甲酸酯的检测进行了探讨。
关键词 食品 食品包装材料 邻苯二甲酸酯 测定
1. 前言
邻苯二甲酸酯是一种用于塑胶产品的增塑剂,目的是增加产品的柔软度,因此对生产柔性PVC产品是十分必要的一种原料。目前中国市场上销售的瓶装产品使用的瓶盖,里面的垫圈大多是加了邻苯二甲酸酯的。早在1982年,美国国家癌症研究所就对邻苯二甲酸酯的致癌性进行了生物鉴定,其结论是:邻苯二甲酸酯是大鼠和小鼠的致癌物,能使啮类动物的肝脏致癌。基于此,各国很早已经在不同程度上限制和禁止邻苯二甲酸酯的使用。前不久,苏黎世州检验中心在对亚洲食品进行检测后,于2007年6月对包括中国某品牌产品在内的10种亚洲食品实施禁售。这些食品为油浸式食物,采用玻璃罐装、金属旋盖式包装,为了密封而内加塑胶圈。PVC垫圈是导致多个亚洲产品被禁售的罪魁祸首。
2005年7月5日,欧洲议会投票通过议案禁止在儿童玩具及用品中使用三种邻苯二甲酸酯类增塑剂,并限制另外三种邻苯二甲酸酯类增塑剂在玩具中的使用;2005年10月25日,国家质检总局的一纸公告终结了己二酸二乙基己酯(DEHA)在PVC保鲜膜中的使用;2005年12月,德国《生态测试》杂志公布了对30种玩具的最新检测报告,宣称在包括芭比娃娃在内的24种玩具中发现了邻苯二甲酸酯类物质。
增塑剂是塑料助剂中最大的品种之一,目前全球增塑剂品种多达200多种,增塑剂在为人类提供高品质塑料制品中的作用不可或缺,正确使用增塑剂是该行业能否健康发展的关键,提高邻苯二甲酸酯的检测能力也变得十分重要。
2. 实验部分
2.1 原理
各类食品经提取、净化后,经气相色谱-质谱联用仪器测定。采用特征选择离子(SIM)碎片的丰度比定性,其丰度比与标准品相比最大相差≤15%,以标准样品定量离子外标法定量。
2.2 试剂
本方法所用水均为全玻璃重蒸馏水,试剂均为重蒸馏分析纯(或色谱纯),储存于玻璃瓶中。
2.2.1 正己烷;
2.2.2 乙腈;
2.2.3 丙酮;
2.2.4 弗罗里硅土:层析用,200℃烘3h后备用;
2.2.5 硅胶键合氨基吸附剂(PSA);
2.2.6 无水硫酸钠:分析纯,200℃烘3h后备用;
2.2.7 氯化钠:分析纯,200℃烘3h后备用;
2.2.8 16种邻苯二甲酸酯标准品:
邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二异丁酯(DIBP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二(2-甲氧基)乙酯(DMEP)、邻苯二甲酸二(4-甲基-2-戊基)酯(BMPP)、邻苯二甲酸二(2-乙氧基)乙酯(DEEP)、邻苯二甲酸二戊酯(DPP)、邻苯二甲酸二己酯(DHXP)、邻苯二甲酸苄基丁基酯(BBP)、邻苯二甲酸二(2-丁氧基)乙酯(DBEP)、邻苯二甲酸二环己酯(DCHP)、邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸二苯酯、邻苯二甲酸二正辛酯(DNOP)、邻苯二甲酸二壬酯(DNP)。纯度均在95%以上。
2.2.9标准储备液:称取上述各种标准品(精确至0.1mg),用正己烷配制成1000mg/L的储备液,于4℃冰箱中避光保存;
2.2.10标准使用液:将16种标准储备液用正己烷稀释成50mg/L的混合标准使用液,再用正己烷将其稀释成0.5、1.0、2.0、4.0、8.0mg/L的混合标准使用液待用。
2.3 仪器
2.3.1 气相色谱-质谱联用仪(GC-MS);
2.3.2 旋转蒸发器;
2.3.3 离心机;
2.3.4 玻璃层析柱:30cm×1.0cm(i.d.);
2.3.5 超声波发生器;
2.3.6 分液漏斗(500mL,125mL);
2.3.7 均质机;
2.3.8 其他玻璃器皿(茄形瓶,离心试管等)。
注:所用玻璃器皿洗净后均用重蒸水洗三次,200℃烘2小时,冷却至室温备用。
2.4 分析步骤
2.4.1 试样处理
2.4.1.1 食品
2.4.1.1.1油脂类固体或半固体样品
称取均匀样品2g(精确至0.1mg)置于离心试管,加入10mL正己烷,均质2min,2500r/min离心3min,己烷层转入125mL分液漏斗,再用10mL正己烷重复提取一次,己烷层并入125mL分液漏斗。依次用30mL、
30mL、30mL乙腈提取三次。合并三次乙腈提取液转入500mL分液漏斗中,加入250mL10%氯化钠溶液,用100mL、100mL正己烷提取两次,经装有10g无水硫酸钠的漏斗收集于茄形瓶,40℃下蒸发至接近干。残留物用5ml正己烷溶解,待过柱用。
2.4.1.1.2油脂类液体样品
称取均匀样品1g(精确至0.1mg)于小烧杯,加入20mL正己烷充分溶解,转入125mL分液漏斗,用30mL乙腈洗烧杯后也转入分液漏斗,后续处理按2.4.1.1.1进行。
2.4.1.1.3不含油脂的固体或半固体样品
称取混匀试样5.00g,置于50mL的玻璃离心试管中,加适量水(使总水量约10mL),加入20mL丙酮+正己烷混合液(2+3),均质2min,2500r/min离心3min,取上层清液经装有5g无水硫酸钠的漏斗收集于茄形瓶。再用20mL正己烷提取一次,合并提取液40℃下蒸发至接近干(若含油和色素较多按2.4.1.1.1过柱净化),用正己烷定容至2mL,待分析。
2.4.1.1.4 不含油脂的液体样品(不含啤酒)
称取均匀样品20g,置于100mL具塞量筒中,加入10mL饱和食盐水,再加入30mL正己烷剧烈振摇,静置分层,上清液经装有5g无水硫酸钠的漏斗收集于茄形瓶,再用30mL正己烷重复提取一次,合并上清液,40℃下蒸发至接近干(若含色素较多按2.4.1.1.1过柱净化),用正己烷定容至2mL,待分析。
2.4.1.1.5 啤酒
称样20g,置于100mL具塞量筒中,加入10mL饱和食盐水,加入20mL乙腈,再加入20mL正己烷剧烈振摇,静置分层,上清液经装有5g无水硫酸钠的漏斗收集于茄形瓶,再用20mL、20mL正己烷重复提取两次,合并上清液,40℃下蒸发至接近干,用正己烷定容至2mL,待分析。
2.4.1.2 食品包装材料
称取经粉碎混匀的试样0.2g(精确至0.1mg)于三角瓶,加入50ml正己烷,超声提取30min,取上清液直接进行分析(视含量作相应的稀释或浓缩)。
2.4.2 净化
2.4.2.1层析柱的制备:玻璃层析柱底部放入少许脱脂棉,加入1cm高的无水硫酸钠,然后依次干法装入2g弗罗里硅土(3.4),0.5gPSA(3.5),上部再加入1cm高的无水硫酸钠。使用前依次用10mL丙酮、10mL正己烷预淋洗。
2.4.2.2净化与浓缩:待淋洗液(正己烷)下降至无水硫酸钠层时,将试样提取液加入,再用5mL正己烷洗茄形瓶,洗液加入层析柱,待其下降至无水硫酸钠层时,用25mL丙酮+正己烷(2+98)混合液洗脱,将洗脱液收集于25mL(视样品中邻苯二甲酸酯含量而定)的容量瓶中,用正己烷定容,待分析。
2.4.3测定
2.4.3.1 色谱条件
色谱柱:HP-5MS石英毛细管柱(30m×0.25mmi.d.×0.25μm),或相当型号固定相色谱柱;
进样口温度:280℃;
升温程序:初始温度60℃,保持1min,以20℃/min的速度升至220℃,保持1min,再以5℃/min的速度升至280℃,保持4min;
载气:氦气;流速:1ml/min;
进样量:1ul不分流进样;
接口温度:280℃;
电离模式:电子轰击源(EI),能量为70eV;
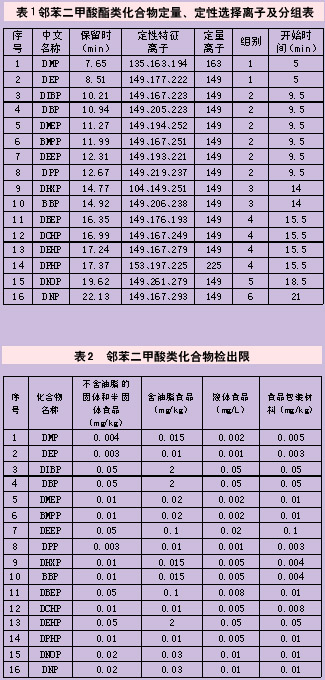
扫描方式:采用选择离子扫描(SIM)采集,特征离子及定量离子及分组情况见表1;
溶剂延迟:5min。
2.4.3.2 结果计算
食品及食品包装材料中邻苯二甲酸酯化合物的含量(mg/kg):
式中:
X——试样中某种邻苯二甲酸酯的含量(mg/kg)
V——试样定容体积(ml)
C1——试样中某种邻苯二甲酸酯峰面积对应的标准品组分的浓度(mg/L)
C0——空白试样中某种邻苯二甲酸酯峰面积对应的标准品组分的浓度(mg/L)
m——试样质量(g)
方法检出限见表2
3 .讨论
(1)对于不含油脂的固体或半固体样品,仅用正己烷作提取溶剂效果不如丙酮和正己烷的混合液,通过实验最终选择丙酮+正己烷混合液(2+3)作为提取溶剂。(2)对于啤酒,加入饱和食盐水后用正己烷直接提取发现乳化现象严重,加入适量乙腈则可以大大改善这种现象。(3)由于实验室中有大量塑料器皿,所以在整个实验过程中要防止其使用,以免发生干扰。

 您当前位置:
您当前位置:





