中国质量新闻网讯 据国家药品监督管理局食品药品审核查验中心近日发布的《医疗器械飞行检查情况通告(2022年第2号)》,上海倍尔康生物医学科技有限公司等7家企业存在一般项目不符合《医疗器械生产质量管理规范》及相关附录要求。
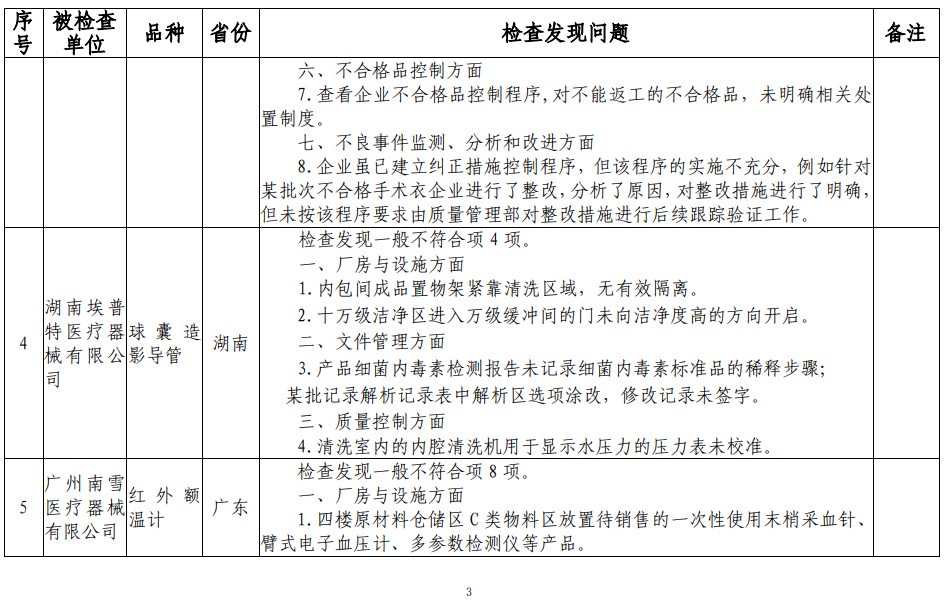
据通告,按照国家药品监督管理局2021年医疗器械检查工作部署,核查中心于2021年10月-12月组织开展了医疗器械生产企业飞行检查工作,发现上海倍尔康生物医学科技有限公司、无锡市宇寿医疗器械有限公司、新乡市康民卫材开发有限公司、湖南埃普特医疗器械有限公司、广州南雪医疗器械有限公司、桂林三金大健康产业有限公司、重庆双双卫生材料有限公司等7家企业存在一般项目不符合《医疗器械生产质量管理规范》及相关附录要求。
针对检查中发现的不符合要求问题,请相关省、自治区、直辖市药品监督管理局督促企业按要求限期整改,要求企业评估产品安全风险,对存在安全风险的,应按照《医疗器械召回管理办法》召回相关产品。企业完成整改后,相关省级药品监督管理局应及时组织对整改情况进行确认,并将确认结果报送国家药品监督管理局食品药品审核查验中心。






 您当前位置:
您当前位置:





